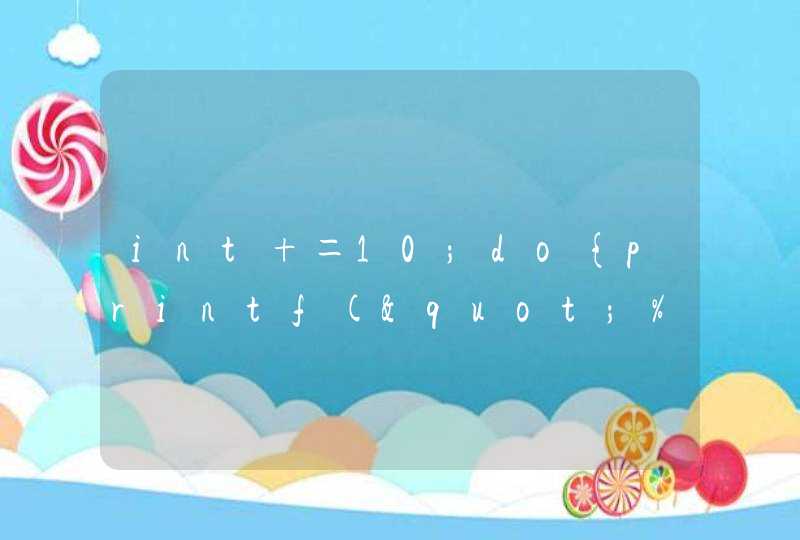其实用方式类似于 circos.track() 函数,可以使用 panel.fun 添加自定义的绘图函数
在 panel.fun 函数中,可以基础图形函数来添加图形,函数接收两个参数 region 和 value :
其中 region 的数据用于标识 x 轴, value 标识的是 y 轴。
panel.fun 函数还强制要求传入第三个参数 ... ,用于传递用户不可见的变量,并交由其内部的基础绘图函数进行解析,如 circos.genomicPoints
例如,我们创建包含两列额外值的数据
我们可以在 panel.fun 函数中,将 region 和 value 打印出来
可以看到, region 为数据的 2 、 3 两列, value 为 4 、 5 两列
numeric.column 参数用于指定 y 轴数据,可以传递对应的列名或列索引,默认为所有数值列(从第四列开始),这些数据拥有相同的 x 轴坐标,可以使用 ylim 来设置数据范围,例如
如果输入数据是数据框列表,则 numeric.column 为长度与列表一致的向量或一个标量
circos.genomicPoints() 用于绘制点图,是使用 circos.points() 函数来实现的
如果你不想使用 circos.genomic*() 类型的函数,可以使用 circos.*() 来实现。
使用方式包括
其他基因组数据绘图函数也是使用对应的 circos.*() 来实现的
因为矩形框的左右边界由 x 轴固定了,只需要设置上下边界即可,参数可以是 ytop , ybottom 或 ytop.column 、 ybottom.column 指定对应的数据列
需要两个数据框来确定连接区域,其他参数都由 circos.link() 解析,例如
circos.genomicTrack() 函数和 panel.fu n 参数对不同的输入数据或不同的模式,会有不同的表现形式
如果输入数据是数据框,绘制方式与前面一样
对于数据框列表的输入数据, panel.fun 将按照当前染色体的各不同数据框进行绘制, region 和 value 表示的是当前染色体,当前数据框所对应的值。
需要在 panel.fun 函数内部使用 getI(...) 来获取当前数据框的索引。例如
在 circos.genomicTrack() 函数中设置 stack = TRUE ,开启堆叠模式。
在堆叠模式下, ylim 将会被重新定义, y 轴将会被分割为一些高度相同的 bin ( y = 1, 2, ... ),每个 bin 内放置对应的图形
如果在堆叠模式下输入数据是包含多列数值列的数据框,则 numeric.column 所指定的每个数值列都会作为一个单元, ylim 被设置为 (0.5,0.5+n) , n 为数值列的数目。 y 轴的值 value 将会被替换为 y=i
例如
如果输入的是数据框列表,则每个数据框被认为是一个单元, ylim 被重定义为 (0.5,0.5+n) , n 为数据框列表的长度。
panel.fun 将会应用在每个数据框中,
为了更容易看出图形的区别,我们只显示一条染色体,并将其绘制成 1/4 圆
添加轨迹 A ,只绘制点
添加轨迹 B ,将点以 stack 模式排列,并添加一条虚线
添加轨迹 C ,使用数据框列表,两个数据框的点设置不同的颜色
添加轨迹 D ,为数据框列表使用堆积的方式
添加轨迹 E ,数据框包含 4 列数值数据,每列数据拥有相同的 x 轴坐标,并设置不同的颜色
添加轨迹 F ,堆叠方式显示 4 列数据
类似于上面的点图,我们也只用 1/4 圆来绘制 chr1
轨迹 A ,绘制简单折线,折线的点为区间中点
轨迹 B ,面积折线图,轨迹 C 为 h 类型
轨迹 D ,用数据框列表绘制分组折线图,每组为一个数据框
轨迹 E ,使用堆叠的方式绘制数据框列表
轨迹 F ,包含 4 列的数据框,绘制分组折线图,每组表示一列
轨迹 G ,堆叠的数据框
轨迹 H ,绘制 segment 类型的线
由于矩阵的颜色表示的值大小,我们定义连续型颜色映射
如果要绘制热图,可以设置 stack 模式
在轨迹 B 中,使用数据框列表的堆叠模式
在轨迹 C 中,我们使用正常的模式实现类似的功能
轨迹 D ,我们可以设置条形的高度, ytop.column = 1 表示 value 的第一列
热图(heatmap)在生信领域基本就是常规操作,基本技能,入门操作。能画热图的工具也有很多,我自己常用的R包是pheatmap。 最近经常看见环状的热图,所以就搜了一下资料学习一下,测试一下。环状热图我也经常会在论文中看到,用法和热图相同,但更适合于需要展示较多基因(数据)时来使用。 ===安装===== install.packages("circlize") install.packages("ComplexHeatmap") library('ComplexHeatmap') library('circlize') ===测试=== data<-read.table("expression.txt",header=T,row.names=1) head(data)//转化为矩阵并对其进行归一化 madt<-as.matrix(data) madt2<-t(scale(t(madt))) Heatmap(madt2) //这就是默认参数,普通的热图range(madt2) //查看值的分布 mycol=colorRamp2(c(-1.7, 0.3, 2.3),c("blue", "white", "red")) //定义颜色范围 circos.heatmap(madt2,col=mycol) //默认参数注: circos.clear() //绘制完成后需要使用此函数完全清除布局 circos.par(gap.after=c(50)) //调整圆环首尾间的距离,数值越大,距离越宽circos.heatmap(madt2,col=mycol, dend.side="inside",rownames.side="outside",rownames.col="black",rownames.cex=0.9,rownames.font=1,cluster=TRUE) 注:dend.side:控制行聚类树的方向,inside为显示在圆环内圈,outside为显示在圆环外圈 #rownames.side:控制矩阵行名的方向,与dend.side相同;但注意二者不能在同一侧,必须一内一外 #cluster=TRUE为对行聚类,cluster=FALSE则不显示聚类下面是换了inside和outside的结果:===聚类树的调整和美化(需要用到两个别的包)=== install.packages("dendextend") //改颜色 install.packages("dendsort") //聚类树回调 library(dendextend) library(dendsort) circos.par(gap.after=c(50)) circos.heatmap(madt2,col=mycol,dend.side="inside",rownames.side="outside",track.height=0.38,rownames.col="black",rownames.cex=0.9,rownames.font=1,cluster=TRUE,dend.track.height=0.18,dend.callback=function(dend,m,si){color_branches(dend,k=15,col=1:15)}) 注:track.height:轨道的高度,数值越大圆环越粗 dend.track.height:调整行聚类树的高度 dend.callback:用于聚类树的回调,当需要对聚类树进行重新排序,或者添加颜色时使用 包含的三个参数:dend:当前扇区的树状图;m:当前扇区对应的子矩阵;si:当前扇区的名称 color_branches():修改聚类树颜色 circos.clear()//添加图例标签等 lg=Legend(title="Exp",col_fun=mycol,direction= c("vertical")) grid.draw(lg)//添加列名 circos.track(track.index=get.current.track.index(),panel.fun=function(x,y) { if(CELL_META$sector.numeric.index==1) { cn=colnames(madt2) n=length(cn) circos.text(rep(CELL_META$cell.xlim[2],n)+convert_x(0.3,"mm"), //x坐标4.1+(1:n)*0.7, //y坐标和间距cn,cex=0.8,adj=c(0,1),facing="inside") } },bg.border=NA)mycol2=colorRamp2(c(-1.7, 0.5, 2.3),c("#57ab81", "white", "#ff9600")) 也可以更改上面的颜色,从而改变热图的配色:===分组热图绘制======== #circos.heatmap()内只能是一个矩阵,但如果矩阵数据存在分组,可以用split参数来指定分类变量 split = sample(letters[1:2], 40, replace = TRUE) split = factor(split, levels = letters[1:2]) circos.clear() circos.par(gap.after=c(22)) circos.heatmap(madt2,col=mycol,split=split,dend.side="inside",rownames.side="outside",track.height = 0.38, rownames.col="black",rownames.cex=0.9, rownames.font=1, cluster=TRUE, dend.track.height=0.18, dend.callback=function(dend,m,si) { color_branches(dend,k=15,col=1:15) } )//假设有两个热图的矩阵数据 madt2<-t(scale(t(madt))) madt3<-t(scale(t(madt))) split2 = sample(letters[1:2], 40, replace = TRUE) split2 = factor(split2, levels = letters[1:2]) circos.clear() circos.par(gap.after=c(8)) circos.heatmap(madt2,col=mycol2,split=split2,dend.side="outside", cluster=TRUE, dend.track.height=0.2, dend.callback=function(dend,m,si) { color_branches(dend,k=15,col=1:15) } ) circos.heatmap(madt3, col = mycol,rownames.side="inside",rownames.cex=0.8)相信大家都听说过circos图,但是亲自画过的人可能就很少,这主要因为软件的安装和使用稍微有一点麻烦。其实,circos图也是可以在线绘制的,这样就简单多了!一起来了解一下吧!
在circos官网(http://circos.ca/)的最右方有个“CIRCOS ONLINE”选项,这里可以实现在线绘制部分circos图。
打开后界面如下:
以微生物多样性分析中样品与物种丰度circos图绘制为例,给大家讲解circos图的绘制功能。该图能够很直观的反映各样品中不同物种所占的比例,以及物种在不同分组或者样品中的分布关系。
绘制circos图
1.数据准备
首先我们要做的就是准备画图所用到的数据,所用数据为物种在各样品中的相对丰度,这里只选用丰度大于0.01的物种用于绘图,数据如下(列名A、B、C为样品,行名Acetobacteraceae等是科一水平的物种分类):
OTUABC
Acetobacteraceae0.5063653216696110.5968872412369940.457528142134733
Arcobacteraceae0.0003294904846044670.0179133872520980.000426249200782749
Bacteroidaceae0.01752092807693420.04558718113953470.352221339584988
Dysgonomonadaceae0.001842974249051360.02565003004872960.0330226880824598
Lachnospiraceae0.005691857602178260.01390206286339050.0173870923992018
Lactobacillaceae0.174952205775860.2379461150250890.0588340146862225
Pseudomonadaceae0.00213263621353880.02862956070929480.0127991010016856
Ruminococcaceae0.003124728441908290.005061219761203110.0274388235522058
Sphingomonadaceae0.2578607015612780.007113946230875610.00898610815104722
由于网站要求的数据格式为非负整数,故将所有的数据乘1000(系统会自动截掉小数点后的数据),输入数据则变为:
OTUABC
Acetobacteraceae506.365321669611596.887241236994457.528142134733
Arcobacteraceae0.32949048460446717.9133872520980.426249200782749
Bacteroidaceae17.520928076934245.5871811395347352.221339584988
Dysgonomonadaceae1.8429742490513625.650030048729633.0226880824598
Lachnospiraceae5.6918576021782613.902062863390517.3870923992018
Lactobacillaceae174.95220577586237.94611502508958.8340146862225
Pseudomonadaceae2.132636213538828.629560709294812.7991010016856
Ruminococcaceae3.124728441908295.0612197612031127.4388235522058
Sphingomonadaceae257.8607015612787.113946230875618.98610815104722
2.绘图
数据准备好就可以来绘制circos图了,只需要导入数据就可以。
生成的图片如下:
可以看到,图中的物种和样品完全是按照字母顺序排列的,我们希望物种和样品分别位列两边,这里可以人为的对其指定顺序。方法也很简单,就是在数据的第一行和第一列用数字来指定顺序。如下:
OTUOTU1 2 3
OTUOTUABC
12Acetobacteraceae506.365321669611596.887241236994457.528142134733
10Bacteroidaceae17.520928076934245.5871811395347352.221339584988
8Dysgonomonadaceae1.8429742490513625.650030048729633.0226880824598
6Lachnospiraceae5.6918576021782613.902062863390517.3870923992018
11Lactobacillaceae174.95220577586237.94611502508958.8340146862225
7Pseudomonadaceae2.132636213538828.629560709294812.7991010016856
5Ruminococcaceae3.124728441908295.0612197612031127.4388235522058
9Sphingomonadaceae257.8607015612787.113946230875618.98610815104722
4Arcobacteraceae0.32949048460446717.9133872520980.426249200782749
第一行指定了样品的顺序,而第一列按丰度指定物种的顺序。生成图片时要勾选下图红框中的选项(排序所用),不然会报错哦!
新图如下:
图中由于部分物种丰度较低,导致物种名重叠,解决这个问题可以改变文字的布局。这时就需要进行设置了。
3.图片设置
点击"settings"进入设置界面,会有很多的设置选项,可以对图片进行细调。
这里只需要修改两个地方即可,将下图第一个红框改为“no”,可以调整文字为垂直布局,避免重叠;但是如果物种名太长,又可能会超出图片范围,所以要缩小圆圈的半径,即将第二个红框改为small。
修改并保存设置后,重新生成图片:
好了,今天我就先给大家介绍到这里,希望对您的科研能有所帮助!祝您工作生活顺心快乐!
更多生物信息课程:
1. 文章越来越难发?是你没发现新思路,基因家族分析发2-4分文章简单快速,学习链接: 基因家族分析实操课程 、 基因家族文献思路解读
2. 转录组数据理解不深入?图表看不懂?点击链接学习深入解读数据结果文件,学习链接: 转录组(有参)结果解读 ; 转录组(无参)结果解读
3. 转录组数据深入挖掘技能-WGCNA,提升你的文章档次,学习链接: WGCNA-加权基因共表达网络分析
4. 转录组数据怎么挖掘?学习链接: 转录组标准分析后的数据挖掘 、 转录组文献解读
5. 微生物16S/ITS/18S分析原理及结果解读 、 OTU网络图绘制 、 cytoscape与网络图绘制课程
6. 生物信息入门到精通必修基础课,学习链接: linux系统使用 、 perl入门到精通 、 perl语言高级 、 R语言画图
7. 医学相关数据挖掘课程,不用做实验也能发文章,学习链接: TCGA-差异基因分析 、 GEO芯片数据挖掘 、 GSEA富集分析课程 、 TCGA临床数据生存分析 、 TCGA-转录因子分析 、 TCGA-ceRNA调控网络分析
8.其他课程链接: 二代测序转录组数据自主分析 、 NCBI数据上传 、 二代测序数据解读 。